
天津師范大學(xué)化學(xué)學(xué)院、智能分子交叉科學(xué)研究院教師張治元副教授和董明副教授在手性大環(huán)的高效合成及識別研究中取得進(jìn)展,相關(guān)成果以“Chiral Macrocycles for Enantioselective Recognition”為題,在線發(fā)表于Journal of the American Chemical Society。
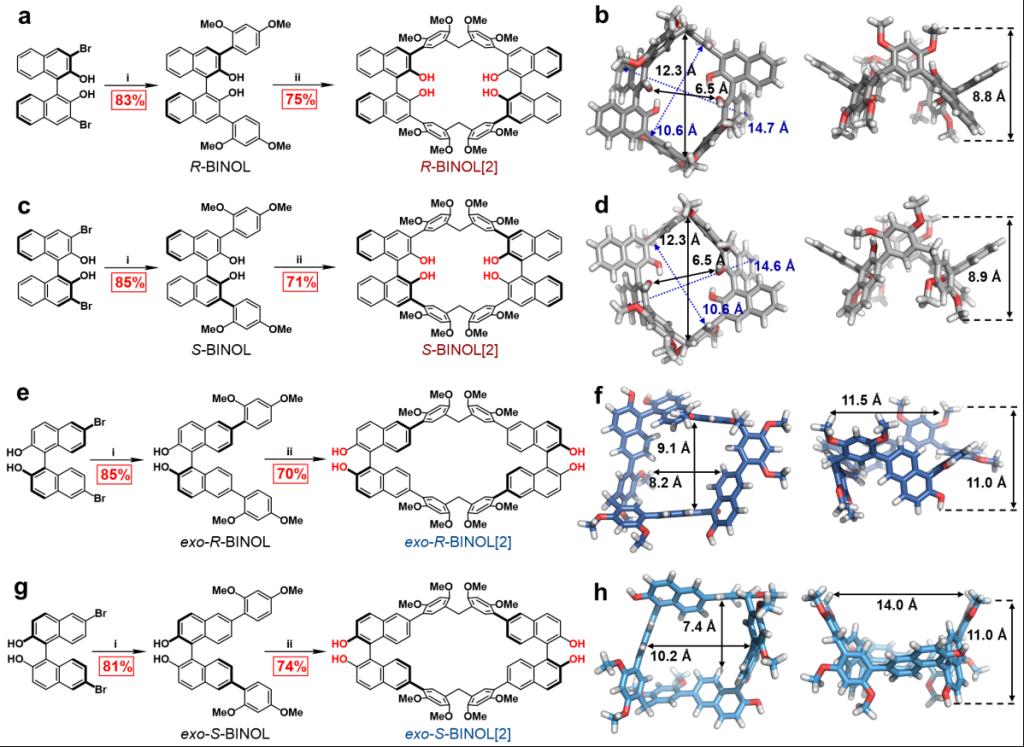
圖 手性聯(lián)萘大環(huán)的合成路線及單晶結(jié)構(gòu)
手性識別對于理解生物過程、輔助藥物設(shè)計(jì)、研發(fā)不對稱催化體系和制備手性分離材料至關(guān)重要。已經(jīng)有多種手性識別工具見諸報(bào)道,包括手性有機(jī)小分子、螺旋超分子組裝體、手性多孔材料和手性聚合物等。手性大環(huán)化合物具有預(yù)組織空腔和多重絡(luò)合位點(diǎn),因而在手性識別方面具有顯著優(yōu)勢,比如手性冠醚、環(huán)糊精、杯芳烴、衍生葫蘆脲和其他手性大環(huán)主體等。然而,現(xiàn)有手性識別體系仍有一些關(guān)鍵問題尚待解決。首先,對映選擇性(KR(S)/KS(R) 或 KL(D)/KD(L))是衡量大環(huán)手性識別能力的關(guān)鍵參數(shù),但是大多數(shù)手性大環(huán)主體對客體的對映選擇性小于5。直到最近幾年,才有對映選擇性大于10的大環(huán)被合成出來。其次,手性大環(huán)化合物的制備通常受限于冗長的合成步驟、較低的合成產(chǎn)率(總產(chǎn)率通常低于20%)以及昂貴的手性分離技術(shù)(比如手性色譜柱),阻礙了其應(yīng)用。因此,亟需開發(fā)兼具簡潔合成步驟、高合成產(chǎn)率和高對映選擇性的手性大環(huán)主體。
該團(tuán)隊(duì)采用“模塊化同步構(gòu)造手性骨架和內(nèi)絡(luò)合位點(diǎn)”的研究思路,以商業(yè)購得的手性純二溴聯(lián)萘酚和2,4-二甲氧基苯硼酸為原料,通過Suzuki–Miyaura偶聯(lián)反應(yīng)得到聯(lián)萘單體,產(chǎn)率大于80%。進(jìn)一步在路易斯酸催化下與多聚甲醛縮合得到大環(huán),產(chǎn)率在70%以上。兩步反應(yīng)總產(chǎn)率高達(dá)62%。為了驗(yàn)證OH識別位點(diǎn)的作用,分別合成了OH朝內(nèi)(R/S-BINOL[2])和朝外(exo-R/S-BINOL[2])的兩對手性大環(huán)對映體。進(jìn)一步研究了手性大環(huán)主體對七對手性客體的識別能力,發(fā)現(xiàn)OH朝內(nèi)大環(huán)R/S-BINOL[2]識別客體的對映選擇性最高可達(dá)13.2。研究表明,高對映選擇性主要來自于大環(huán)主體和手性客體之間有利的立體化學(xué)契合,以及多種非共價協(xié)同作用。該工作將為手性化合物的識別和分離提供重要研究工具。
第一作者是天津師范大學(xué)化學(xué)學(xué)院碩士研究生孫光,通訊作者為天津師范大學(xué)化學(xué)學(xué)院、智能分子交叉科學(xué)研究院教師張治元副教授、董明副教授、李春舉教授和美國德克薩斯大學(xué)奧斯汀分校Jonathan L. Sessler教授。該研究工作得到了國家自然科學(xué)基金(21971192, 22201211, 22301218)、天津市自然科學(xué)基金(23JCZDJC00660,20JCZDJC00200)等資金支持。
論文鏈接:https://pubs.acs.org/doi/10.1021/jacs.4c07924